Ada yang tahu pengertian istilah2 diatas?, Mungkin beberapa dari
kita, termasuk saya sendiri begitu dan masih sangat bingung dengan
berbagai per-istilahan dalam bidang kimia.
Istilah – istilah tersebut sebenarnya sering kita dengar.
Saking seringnya mendengar, kita anggap hal tersebut adalah hal lumrah,
sehingga dianggap tidak perlu kita pertanyakan/permasalahkan, bahkan
mungkin kita anggap hal tersebut sebagai hal2 biasa/sepele.
Walaupun begitu, tidak jarang ketika kita ditanya pengertian istilah2 diatas, yang ada malah “TINGTONG”, alias kebingungan, nah lho??.
Belakangan ini sy pun sadar hal itu.
8O “Sadar/dasar emang lo nya aj yg gtw?? ngapain aja dulu sekolah?? “
:mrgreen: terserah ah, yg penting gw masih mau berlajar lagi..
Berikut pengertian & perbedaan Atom, Molekul, Ion, Unsur,
Senyawa, Campuran, yang sy rangkum, juga ta buat oret2annya, mudah2an jd
ngerti. Maaf jika ada penjelasan yang salah/kurang pas, nanti boleh
ditanya ke guru/dosennya ya :)
PARTIKEL PENYUSUN MATERI/ZAT
Partikel adalah sebuah satuan dasar dari benda atau
materi. Bisa juga dikatakan Partikel merupakan satuan bagian terkecil
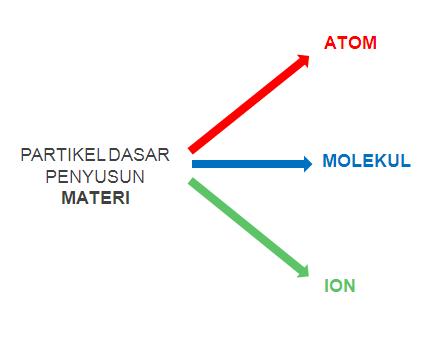
dari suatu materi. Jenis Partikel ini ada 3 yaitu: atom, molekul, dan
ion. Jadi baik atom, molekul, dan ion ke tiga-nya merupakan satuan terkecil dari materi yg secara umum disebut partikel
 1. Atom adalah: Satuan terkecil
dari suatu materi yang terdiri atas inti, yang biasanya mengandung
proton (muatan+) dan neutron (netral), dan kulit yang berisi muatan
negatif yaitu elektron. Ada juga yang menyebutkan bahwa atom adalah
partikel penyusun unsur.
Kedua pengetian ini semuanya benar. Yang pasti atom itu :
– punya proton, neutron, elektron, (kecuali pd Hidrogen-1, yg tidak memiliki neutron)
– punya karekteristik tertentu, yaitu punya jumlah proton dan elektron yang sama (jika tdk sama disebut ion)
– atom2 yang punya karakteristik yang sama dinamakan unsur,
Analogi sederhana: Setiap orang yang sering membaca,
kita sebut sikutu buku, ceritanya kita punya 4 teman yang punya hobi
membaca, sehingga kita simpulkan keempat teman kita ini sikutubuku
karena punya kebiasaan yang sama. Jadi
teman kita= atom,
sama2 hobi baca= punya jumlah proton&elektron sama/ berkarakter sama,
sikutu buku=unsur
Anggapan yang salah
– gabungan/ikatan beberapa atom akan membentuk unsur (SALAH).
Yang benar: unsur adalah nama untuk kumpulan/himpunan atom yang punya
karakter yang sama. Gabungan/ikatan dari beberapa atom bukan membentuk
unsur tapi membentuk molekul. Bedakan himpunan dan ikatan..!
2. Molekul adalah: Gabungan dari
beberapa atom unsur, bisa dua atau lebih. Artinya ketika berbicara
molekul maka yang dibayangkan adalah gabungan atom2 (bukan 1 atom).
Molekul adalah partikel terkecil dari suatu unsur/senyawa
– Jika gabungan dari atom unsur yang sama jenisnya maka disebut Molekul Unsur, Contohnya: O2, H2, O3, S8
– Jika gabungan dari atom unsur yang berbeda jenisnya maka disebut Molekul Senyawa, Contohnya: H2O, CO2, C2H5
3. Ion adalah: atom yang bermuatan listrik, ion yang
bermuatan listrik disebut kation, dan ion yang bermuatan negatif
disebut anion. Kation dan anion dapat berupa ion tunggal hanya terdiri
dari satu jenis atom atau dapat pula berupa ion poliatom mengandung dua
atau lebih atom yang berbeda.
Beberapa Kesimpulan:
Unsur itu partikelnya bisa berupa atom/molekul unsur. Unsur2 yang
partikelnya berupa atom, berarti unsur tersebut bisa berdiri sendiri
atau hanya mengandung satu atom saja, penulisannya ditulis dengan
lambang unsurnya, misalnya C (karbon), He (Helium). Bila partikelnya
berupa molekul maka artinya unsur tersebut dibentuk dari gabungan atom
yang berjenis sama, dia tidak bisa berdiri sendiri, unsur2 tersebut
ditulis dengan lambang unsurnya disertai dengan jumlah atom penyusunya.
Contohnya: O2, H2. Makanya unsur oksigen tidak pernah ditulis hanya
huruf O saja, melainkan ditambah angka 2 sebagai arti bahwa Unsur ini
dibentuk dari 2 atom oksigen.
1. Unsur adalah: Sekelompok atom yang memiliki
jumlah proton yang sama pada intinya. Jumlah ini disebut sebagai nomor
atom unsur. Unsur didefinisikan pula sebagai zat tunggal yang sudah
tidak bisa dibagi-bagi lagi menjadi bagian yang lebih kecil.
1. Atom adalah: Satuan terkecil
dari suatu materi yang terdiri atas inti, yang biasanya mengandung
proton (muatan+) dan neutron (netral), dan kulit yang berisi muatan
negatif yaitu elektron. Ada juga yang menyebutkan bahwa atom adalah
partikel penyusun unsur.
Kedua pengetian ini semuanya benar. Yang pasti atom itu :
– punya proton, neutron, elektron, (kecuali pd Hidrogen-1, yg tidak memiliki neutron)
– punya karekteristik tertentu, yaitu punya jumlah proton dan elektron yang sama (jika tdk sama disebut ion)
– atom2 yang punya karakteristik yang sama dinamakan unsur,
Analogi sederhana: Setiap orang yang sering membaca,
kita sebut sikutu buku, ceritanya kita punya 4 teman yang punya hobi
membaca, sehingga kita simpulkan keempat teman kita ini sikutubuku
karena punya kebiasaan yang sama. Jadi
teman kita= atom,
sama2 hobi baca= punya jumlah proton&elektron sama/ berkarakter sama,
sikutu buku=unsur
Anggapan yang salah
– gabungan/ikatan beberapa atom akan membentuk unsur (SALAH).
Yang benar: unsur adalah nama untuk kumpulan/himpunan atom yang punya
karakter yang sama. Gabungan/ikatan dari beberapa atom bukan membentuk
unsur tapi membentuk molekul. Bedakan himpunan dan ikatan..!
2. Molekul adalah: Gabungan dari
beberapa atom unsur, bisa dua atau lebih. Artinya ketika berbicara
molekul maka yang dibayangkan adalah gabungan atom2 (bukan 1 atom).
Molekul adalah partikel terkecil dari suatu unsur/senyawa
– Jika gabungan dari atom unsur yang sama jenisnya maka disebut Molekul Unsur, Contohnya: O2, H2, O3, S8
– Jika gabungan dari atom unsur yang berbeda jenisnya maka disebut Molekul Senyawa, Contohnya: H2O, CO2, C2H5
3. Ion adalah: atom yang bermuatan listrik, ion yang
bermuatan listrik disebut kation, dan ion yang bermuatan negatif
disebut anion. Kation dan anion dapat berupa ion tunggal hanya terdiri
dari satu jenis atom atau dapat pula berupa ion poliatom mengandung dua
atau lebih atom yang berbeda.
Beberapa Kesimpulan:
Unsur itu partikelnya bisa berupa atom/molekul unsur. Unsur2 yang
partikelnya berupa atom, berarti unsur tersebut bisa berdiri sendiri
atau hanya mengandung satu atom saja, penulisannya ditulis dengan
lambang unsurnya, misalnya C (karbon), He (Helium). Bila partikelnya
berupa molekul maka artinya unsur tersebut dibentuk dari gabungan atom
yang berjenis sama, dia tidak bisa berdiri sendiri, unsur2 tersebut
ditulis dengan lambang unsurnya disertai dengan jumlah atom penyusunya.
Contohnya: O2, H2. Makanya unsur oksigen tidak pernah ditulis hanya
huruf O saja, melainkan ditambah angka 2 sebagai arti bahwa Unsur ini
dibentuk dari 2 atom oksigen.
1. Unsur adalah: Sekelompok atom yang memiliki
jumlah proton yang sama pada intinya. Jumlah ini disebut sebagai nomor
atom unsur. Unsur didefinisikan pula sebagai zat tunggal yang sudah
tidak bisa dibagi-bagi lagi menjadi bagian yang lebih kecil.
Saya hanya ingin menekankan “unsur hanyalah sebutan saja
untuk atom-atom yg yang punya karakter sama (punya jumlah proton yg
sama)”. Sebagai contoh, semua atom yang memiliki 6 proton pada intinya
adalah atom dari unsur kimia karbon, dan semua atom yang memiliki 92
proton pada intinya adalah atom unsur uranium.
Bisa dibilang unsur adalah atom itu sendiri, contohnya: jika ada H2O,
maka kita bisa bilang: terdiri dari 2 atom hidrogen, dan 1 atom
oksigen, padahal Hidrogen dan oksigen keduanya adalah unsur.
2. Senyawa: Senyawa adalah zat tunggal yang terdiri atas beberapa unsur yang saling kait-mengait. Senyawa dibentuk dari minimal 2 unsur yang berbeda.
Walaupun dibentuk dari unsur yang berbeda, namun senyawa tetap disebut
zat tunggal, karena sifat-sifat unsur yang membentuknya tidak dapat di
temukan pada senyawa. Dengan kata lain
Senyawa telah menjelma menjadi zat yang baru.
Contoh:
Reaksi antara Hidrogen(H) dan oksigen (O2), diperoleh zat baru yang disebut air, yaitu:
H + O2 ——–> H2O
Pada reaksi tersebut, dihasilkan zat baru yang sifatnya berbeda dari
unsur-unsur penyusunnya. Hidrogen adalah gas yang sangat ringan dan
mudah terbakar, sedangkan oksigen adalah gas yang terdapat di udara yang
sangat diperlukan tubuh kita untuk pembakaran. Tampak jelas bahwa sifat
air berbeda dengan sifat hidrogen dan oksigen.
Ciri khas senyawa adalah dia mempunyai perbandingan massa penyusun
yang tetap, air tersusun dari oksigen dan hidrogen dengan perbandingan
massa unsur oksigen banding hidrogen adalah selalu 8 : 1
Perbedaan Senyawa dan molekul
“setiap senyawa adalah molekul namun setiap molekul belum tentu
senyawa”. Senyawa adalah gabungan minimal 2 atom berbeda, sedangkan
molekul gabungan minimal 2 atom bisa sama bisa juga berbeda.
3. Campuran: Zat yang tersusun dari beberapa zat
yang lain jenis dan tidak tetap susunannya dari unsur dan senyawa.
Campuran merupakan materi yang terdiri dari dua atau zat tunggal. Materi
yang kita jumpai sehari-hari hampir semuanya campuran. Bahkan kita
sering membuat campuran bahan, misalnya ketika kita membuat kopi atau
teh manis.
Campuran dibedakan menjadi tiga jenis, yaitu:
- Campuran homogen = Larutan
- Campuran Heterogen = Suspensi, dan
- Campuran yang keadaannya antara suspensi dan larutan = Koloid
1.PENGERTIAN ATOM DAN TEORI-TEORI TENTANG ATOM
Atom berasal
dari kata "atomos"(Yunani) yang berarti tidak dapat di bagi lagi.Sesuai
pengertian tersebut,atom adalah penyusun semua benda yang berukuran
sangat kecil.Benda sehari-hari yang kita temui terdiri dari atom-atom.
Materi atom ini terbentuk karena adanya interaksi dari partikel
subatom(sebuah inti atom dari beberapa proton dan neutron, serta awan
dari garis edar elektron-elektron).Terus apa itu materi?gimana sih
bentuknya?sebenranya materi itu sering kita jumpai,bahkan kita
sentuh,tapi kita belum menyadarinya.Dalam ilmu kimia, Materi adalah
segala sesuatu yang mempunyai massa, menempati volume, dan mempunyai
sifat dapat dilihat, dicium, didengar, dirasa, dan dapat diraba.Materi
tersusun atas molekul-molekul, dan molekul pun tersusun atas atom-atom.
Materi umumnya dapat dijumpai dalam empat fase berbeda, yaitu padat,
cairan, gas, dan plasma (wujud zat). Namun, terdapat pula fase materi
yang lain, seperti kondensat Bose-Einstein.Batu; Pasir; Udara; air;
oksigen; Nitrogen; Radio; Televisi; Kursi; pakaian; .dll itu semua
adalah materi dalam ilmu kimia.
Atom juga terdir dari beberapa sub atom yaitu
-proton(atom yang bermuatan positif)
-elektron(atom yang bermuatan negatif)
-neutron(atom yang tidak bermuatan)
Dasar-dasar
adanya atom ini berasal dari teori yang dikemukakan oleh John Dalton
(1766-1844). Dalton mengatakan bahwa semua unsur kimia tersusun atas
partikel-partikel yang sangat kecil, yang disebut atom, yang tidak bisa
pecah saat zat-zat kimianya direaksikan.
Adapun pendapat lain dari John Dalton adalah
A.Setiap unsur terdiri atas partikel-partikel terkecil yang tak dapat dibagi-bagi lagi, disebut atom.
B.Atom
di gambarkan sebagai bola pejal yang sangat kecil.suatu unsur memiliki
atom-atom yang identik dan berbeda untuk unsur yang berbeda.
C.Atom-atom
bergabung membentuk senyawa dengan perbandingan bilangan bulat dan
sederhana. Misalnya air terdiri dari atom-atom hidrogen dan atom-atom
oksigen
D.Reaksi kimia merupakan pemisahan, penggabungan atau
penyusunan kembali atom- atom, sehingga atom tidak dapat diciptakan atau
dimusnahkan.Hipotesis Dalton digambarkan dengan model atom sebagai bola
pejal seperti bola tolak peluru.
KELEBIHAN TEORI ATOM DHALTON
teori
atom dalton merupakan teori pokok yang membuat ilmuan lain
tergeleng-geleng untuk mempelajari atom secara lebih mendalam sehingga
muncul mide-model atom yang lebih kompleks.
KELEMAHAN TEORI ATOM DHALTON
1.model atom dalton tidak dapat menjelaskan sifat listrik dari materi.
2.model
atom dalton tidak dapat menjelaskan perbedaan antar atom yang satu
dengan atom yang lain.
3model atom dalton tidak dapat menjelaskan bagaimana cara atom saling
berkaitan.Contohnya ikatan antara 2 atom hidrogen dan oksigen
membentuk senyawa H2O(AIR)
3.atom sebenarnya dapat dilainkan
membikin partkel yang kian kecil., hal ini tentunya bertentangan dengan
yang dikemukakan teori dalton bahwa atom tidak dapat dibagi lagi.
2.teori
atom menurut j.j. thompson
Seorang fisikawan Inggris, Joseph John Thomson, pada 1897 menemukan
elektron, suatu partikel bermuatan negatif yang lebih ringan daripada
atom. Dia memperlihatkan bahwa elektron merupakan partikel subatomik.
Dari penemuannya ini, J. J. Thomson mengemukakan dugaan (hipotesis)
sebagai berikut: "karena elektron bermuatan negatif, sedangkan atom
bermuatan listrik netral maka haruslah ada muatan listrik positif yang
mengimbangi muatan elektron dalam atom". Maka ia mengusulkan suatu model
atom yang dikenal dengan model atom roti kismis sebagai berikut.
Atom berbentuk bola pejal bermuatan positif yang homogen
(diibaratkan sebagai roti).
Elektron bermuatan negatif tersebar di dalamnya (seperti kismis yang
tersebar di dalam roti).
Beberapa kelebihan dan kelemahan dari model atom Thomson, dapat dilihat
seperti uraian berikut ini:
Kelebihan Teori Atom Thomson :
Dapat menerangkan adanya partikel yang lebih kecil dari atom yang disebut partikel subatomik.
Dapat menerangkan sifat listrik atom.
Kelemahan Teori Atom Thomson :
Tidak dapat menerangkan fenomena penghamburan partikel alfa oleh selaput tipis emas yang dikemukakan oleh Rutherford.
Tidak
dapat menjelaskan adanya inti atom
3.teori atom rutherfod
A. Teori Atom Rutherford
Setelah diusulkannya teori atom Dalton dan Thomson, muncul teori yang
lebih baru yang digagas oleh Ernerst Rutherford, yang sekarang dikenal
dengan teori atom Rutherford. Pada tahun 1911, Rutherford menyangkal
kebenaran teori atom Thomson yang mengatakan bahwa atom merupakan
bermuatan positif, dan disekelilingnya terdapat elektron bermuatan
negatif layaknya roti kismis.
Atom Rutherford tersusun dari :
- Inti atom yang bermuatan positif
- Elektron-elektron yang bermuatan negatif dan mengelilingi inti.
- Semua proton terkumpul dalam inti atom dan menyebabkan inti atom bermuatan positif.
- Sebagian besar ruangan dalam atom merupakan ruangan kosong/hampa.
-
Jumlah muatan inti sama dengan jumlah muatan elektron sehingga ataom
bersifat netral.
Pengertian Teori atom rutherford
Teori atom Rutherford mengatakan bahwa atom mempunyai inti yang
merupakan pusat massa yang kemudian dinamakan nukleus, dengan
dikelilingi awan elektron bermuatan negatif.
Dasar Teori atom rutherford
Teori atom Rutherford didasarkan pada eksperimen penembakan inti atom
lempengan emas dengan partikel alfa yang dikenal dengan percobaan
Geiger-Marsden. Pada saat itu, Rutherford menysun desain rancangan
percobaan penembakan atom emas oleh partikel alfa yang dipancarkan oleh
unsur radioaktif. Ternyata, sinar radioaktf tersebut ada yang
dipantulkan, dibelokkan, dan
diteruskan.
Dari penjabaran di atas, maka sekiranya model atom Rutherford dapat
disimpulkan sebagai berikut:
Sebagian besar volume atom
merupakan ruang hampa.
Massa atom terpusat di inti atom.
Muatan atom terkonsentrasi pada pusat atom dengan volume yang sangat
kecil. Kelipatan muatan ini sebanding dengan massa atom.
Awan elektron tidak mempengaruhi penyebaran partikel alfa.
B. Kelebihan dan Kelemahan Atom Rutherford
I. Kelebihan Atom Rutherford
Bahwa atom memiliki inti atom yang bermuatan positif dan disekelilingnya terdapat elektron yang mengelilinya.
Dapat menerangkan fenomena penghamburan partikel alfa oleh selaput tipis emas
Jari-jari inti atom dan jari-jari atom sudah dapat ditemukan
Sudah dapat menerangkan / menentukan bentuk lintasan elektron yang mengelilingi inti atom
Dapat menggambarkan gerak elektron disekitar inti
Elektron dapat bergerak dalam lintasan apapun, dari lintasan yang tak terhingga jumlahnya
II.
Kekurangan Atom Rutherford
Model atom rutherford ini belum mampu menjelaskan dimana letak
elektron dan cara rotasinya terhadap ini atom.
Elektron memancarkan energi ketika bergerak, sehingga energi atom
menjadi tidak stabil.
Tidak dapat menjelaskan spektrum garis pada atom hidrogen (H).
Tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti
atom. Berdasarkan teori fisika, gerakan elektron mengelilingi inti ini
disertai pemancaran energi sehingga lama-kelamaan energi elektron akan
berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke
dalam inti.
4.Model Atom Bohr
Model Bohr dari atom hidrogen menggambarkan elektron-elektron bermuatan
negatif mengorbit pada kulit atom dalam lintasan tertentu mengelilingi
inti atom yang bermuatan positif. Ketika elektron meloncat dari satu
orbit ke orbit lainnya selalu disertai dengan pemancaran atau penyerapan
sejumlah energi elektromagnetik hf.
Menurut Bohr :
”Ada aturan fisika kuantum yang hanya mengizinkan sejumlah tertentu
elektron dalam tiap orbit. Hanya ada ruang untuk dua elektron dalam
orbit terdekat dari inti. (John Gribbin, 2005)”
Model Bohr dari atom hidrogen menggambarkan elektron-elektron bermuatan
negatif mengorbit pada kulit atom dalam lintasan tertentu mengelilingi
inti atom yang bermuatan positif. Ketika elektron meloncat dari satu
orbit ke orbit lainnya selalu disertai dengan pemancaran atau penyerapan
sejumlah energi elektromagnetik hf.
Model ini adalah pengembangan dari model puding prem (1904), model
Saturnian (1904), dan model Rutherford (1911). Karena model Bohr adalah
pengembangan dari model Rutherford, banyak sumber mengkombinasikan kedua
nama dalam penyebutannya menjadi model Rutherford-Bohr.
Kunci sukses model ini adalah dalam menjelaskan formula Rydberg mengenai
garis-garis emisi spektral atom hidrogen, walaupun formula Rydberg
sudah dikenal secara eksperimental, tetapi tidak pernah mendapatkan
landasan teoritis sebelum model Bohr diperkenalkan. Tidak hanya karena
model Bohr menjelaskan alasan untuk struktur formula Rydberg, ia juga
memberikan justifikasi hasil empirisnya dalam hal suku-suku konstanta
fisika fundamental.
Model Bohr adalah sebuah model primitif mengenai atom hidrogen. Sebagai
sebuah teori, model Bohr dapat dianggap sebagai sebuah pendekatan orde
pertama dari atom hidrogen menggunakan mekanika kuantum yang lebih umum
dan akurat, dan dengan demikian dapat dianggap sebagai model yang telah
usang. Namun demikian, karena kesederhanaannya, dan hasil yang tepat
untuk sebuah sistem tertentu, model Bohr tetap diajarkan sebagai
pengenalan pada mekanika kuantum.
Kelemahan teori atom Rutherford yang diperbaiki oleh Neils Bohr yaitu :
a. Elektron-elektron yang mengelilingi inti mempunyai lintasan dan energi tertentu.
b.
Dalam orbital tertentu, energi elektron adalah tetap. Elektron akan
menyerap energi jika berpindah ke orbit yang lebih luar dan akan
membebaskan energi jika berpindah ke orbit yang lebih dalam
Kelebihan model atom Bohr
Atom terdiri dari beberapa kulit/subkulit untuk tempat berpindahnya
electron dan atom membentuk suatu orbit dimana inti atom merupakan
positif dan disekelilingnya terdapat elektron.
Kelemahan model atom Bohr
a. Tidak dapat menjelaskan efek Zeeman dan efek Strack.
b.
Tidak dapat menerangkan kejadian-kejadian dalam ikatan kimia dengan
baik, pengaruh medan magnet terhadap atom-atom, dan spektrum atom yang
berelektron lebih banyak.
5. Teori Atom Mekanika Kuantum
image
Erwin Schrodinger
Spektrum atom dan mekanika kuantum
Bohr merupakan orang yang pertama menghubungkan teori struktur atom
dengan tingkat energi elektron untuk menjelaskan spektrum.
Teori atom Bohr berhasil menjelaskan struktur atom hidrogen, tetapi
belum dapat menerangkan atom berelektron banyak.
Masih ada kekurangan yang mendasar pada model atom Bohr.
Kekurangan model atom Bohr disempurnakan dengan model atom mekanika
kuantum.
Model atom mekanika kuantum dikembangkan oleh Erwin Schrodinger
(1926).Sebelum Erwin Schrodinger, seorang ahli dari Jerman Werner
Heisenberg mengembangkan teori mekanika kuantum yang dikenal dengan
prinsip ketidakpastian yaitu “Tidak mungkin dapat ditentukan kedudukan
dan momentum suatu benda secara seksama pada saat bersamaan, yang dapat
ditentukan adalah kebolehjadian menemukan elektron pada jarak tertentu
dari inti atom”..
Daerah ruang di sekitar inti dengan kebolehjadian untuk mendapatkan
elektron disebut orbital. Bentuk dan tingkat energi orbital dirumuskan
oleh Erwin Schrodinger.
Erwin Schrodinger memecahkan suatu persamaan untuk mendapatkan fungsi
gelombang untuk menggambarkan batas kemungkinan ditemukannya elektron
dalam tiga dimensi.
Persamaan Schrodinger
image
x,y dan z = Posisi dalam tiga dimensi
Y = Fungsi gelombang
m = massa
ђ = h/2p dimana h = konstanta plank dan p = 3,14
E = Energi total
V = Energi potensial
Model atom dengan orbital lintasan elektron ini disebut model atom
modern atau model atom mekanika kuantum yang berlaku sampai saat ini,
seperti terlihat pada gambar berikut ini.
Awan elektron disekitar inti menunjukan tempat kebolehjadian elektron.
Orbital menggambarkan tingkat energi elektron. Orbital-orbital dengan
tingkat energi yang sama atau hampir sama akan membentuk sub kulit.
Beberapa sub kulit bergabung membentuk kulit.
image
Dengan demikian kulit terdiri dari beberapa sub kulit dan subkulit
terdiri dari beberapa orbital. Walaupun posisi kulitnya sama tetapi
posisi orbitalnya belum tentu sama.
Ciri khas model atom mekanika gelombang
Gerakan elektron memiliki sifat gelombang, sehingga lintasannya
(orbitnya) tidak stasioner seperti model Bohr, tetapi mengikuti
penyelesaian kuadrat fungsi gelombang yang disebut orbital (bentuk tiga
dimensi darikebolehjadian paling besar ditemukannya elektron dengan
keadaan tertentu dalam suatu atom)
Bentuk dan ukuran orbital bergantung pada harga dari ketiga bilangan
kuantumnya. (Elektron yang menempati orbital dinyatakan dalam bilangan
kuantum tersebut)
Posisi elektron sejauh 0,529 Amstrong dari inti H menurut Bohr
bukannya sesuatu yang pasti, tetapi bolehjadi merupakan peluang terbesar
ditemukannya elektron.
Bilangan kuantum dan orbital atom
Schrodinger berhasil menyelesaikan seperangkat persamaan matematis
yang menghasilkan tiga bilangan kuantum yang menunjukkan daerah
kebolehjadian menemukan elektron di sekeliling inti.
Ketiga bilangan kuantum itu adalah bilangan kuantum utama (n),
bilangan kuantum azimut (l), dan bilangan kuantum magnetik (ml).
Bilangan kuantum utama (n) menunjukkan tingkat energi.
Bilangan kuantum azimut (l) menentukan bentuk orbital dan sub
tingkatan energi.
Bilangan kuantum magnetik (ml) menyatakan orientasi orbital atau
sikap orbital terhadap orbital lain.
Selain tiga bilangan kuantum yang berasal dari penyelesaian
persamaan Schrodinger, masih ada satu bilangan kuantum, yaitu bilangan
kuantum spin (ms).
Bilangan kuantum spin menentukan arah perputaran (spin) tiap
elektron.
Menggambarkan bentuk orbital s, p, dan d.
Konfigurasi elektron dan sistem periodik
Menurut prinsip Aufbau, konfigurasi elektron dimulai dari subkulit
yang memiliki tingkat energi terendah dan diikuti dengan subkulit yang
memiliki tingkat energi lebih tinggi.
Asas larangan Pauli menyatakan bahwa tidak ada dua elektron dalam
sebuah atom apa pun dapat mempunyai keempat bilangan kuantum yang sama.
Menurut aturan Hund, dalam subtingkatan energi tertentu, tiap
orbitaldihuni oleh satu elektron terlebih dahulu sebelum ada orbital
yang memiliki sepasang elektron. Elektron-elektron tunggal dalam orbital
itu mempunyai spin searah (paralel).
Dalam sistem periodik unsur, unsur dikelompokkan dalam empat blok,
yaitu blok s, blok p, blok d, dan blok f.
ya seperti yang kita tahu saat ini,model mekanika kuantum lah yang
digunakan.Tapi apakah anda tahu?bahwa tuhan itu sangat adil untuk
siapapun dan untuk apapun.ternyata atom model mekanika kuantum ini masih
ada kekuranganya lho!wah apaan ya?
KELEBIHAN
1. Mengetahui dimana keboleh jadian menemukan elektron (orbital)
2. Mengetahui dimana posisi elektron yang sedang mengorbit
3. BIsa ngukur perpindahan energi eksitasi dan emisinya
4.
BIsa teridentifikasi kalau di inti terdapat proton dan netron kemudian
dikelilingi oleh elektron yang berputar diporosnya/ di orbitalnya
KELEMAHAN
Persamaan gelombang Schrodinger hanya dapat diterapkan secara eksak untuk partikel
dalam kotak dan atom dengan elektron tunggal
THANKS
